
近日,海南大学吴锡龙教授团队围绕肿瘤精准消融中的关键瓶颈取得新进展。针对活性氧(ROS)治疗易受肿瘤缺氧微环境抑制、纳米药物难以深入肿瘤内部等难题,团队设计构建了一种光/声/磁三重响应的三元异质纳米晶平台(BPF),将S型异质结、纳米酶催化与外部物理场驱动有机结合,实现了ROS的高效级联放大与深层肿瘤穿透消融,为提升实体瘤治疗效率提供了新的解决思路。
在结构设计上,超薄黑磷纳米片充当压电元件,能将超声波的机械振动转化为电化学能量;金属有机框架PCN-224是一种高效光敏剂,在660纳米红光照射下能激发产生ROS;超顺磁性四氧化三铁纳米粒子则身兼数职—既是Fenton反应的催化剂,又能分解过氧化氢产生氧气缓解肿瘤缺氧,还赋予了整个平台磁靶向和磁共振成像的能力。该平台的核心创新在于引入了S型异质结设计。当黑磷与PCN-224两种半导体紧密接触后,因功函数差异在界面自发形成内建电场,使光照和超声激发产生的电荷载流子沿特定方向“分流”,避免了传统异质结中电子与空穴快速复合的效率损失。实验表明,这种设计使BPF在超声激发下的单线态氧产量达到单一PCN-224的三倍。
在药物递送层面,研究团队采用了超声和磁场的“双引擎”驱动策略。磁场将纳米晶体精准引导至肿瘤区域并使其富集,超声波则通过机械效应松动肿瘤致密的细胞外基质,帮助纳米药物深入肿瘤核心。在模拟实体瘤的三维肿瘤球实验中,双重驱动下BPF的穿透深度和分布均度远超单一驱动。进一步的小鼠黑色素瘤模型系列实验显示,磁场和超声协同驱动可显著促进BPF在肿瘤部位富集并向深部渗透,使其在原位瘤、双侧瘤、复发瘤和肺转移模型中均表现出优异的抑瘤效果。更重要的是,该平台不仅能够增强肿瘤细胞凋亡和免疫原性细胞死亡,还可促进树突状细胞成熟、T细胞浸润及免疫记忆形成,并兼具近红外荧光成像和T2加权MRI双模引导能力。
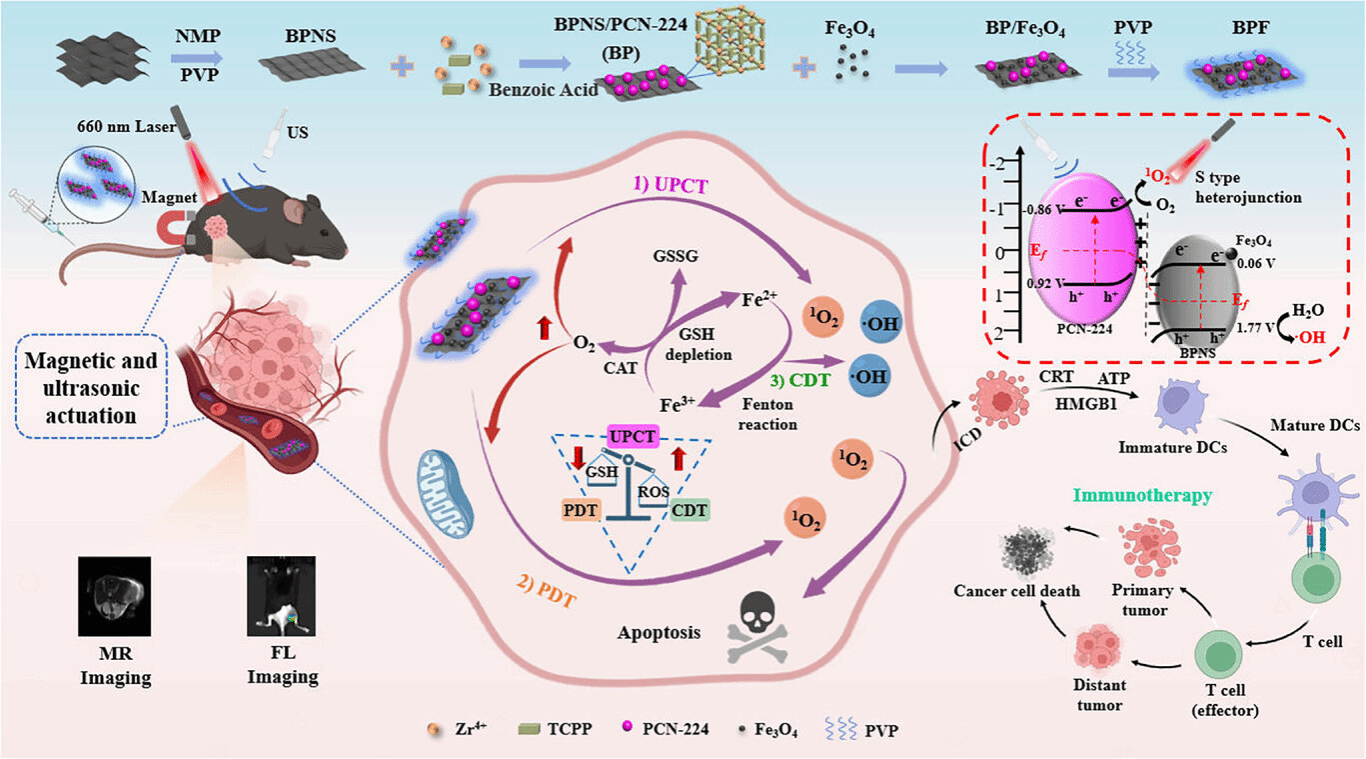
光/声/磁三重响应型三元异质纳米晶BPF的构建及其用于黑色素瘤诊疗示意图
本研究创新性地S型异质结架构引入肿瘤纳米催化治疗领域,整合了压电催化、光敏化和纳米酶催化三种ROS生成途径,为构建兼具高效ROS放大、肿瘤微环境重塑、声磁驱动深层穿透递送和系统性免疫激活功能的新一代纳米治疗平台提供了创新思路。
论文信息:S. Qiu, Y. Wu, R. Liu, et al. Photo/Sono/Magneto-Responsive Ternary Heteronanocrystals with S-Scheme Heterojunction for Penetrative and ROS-Amplified Tumor Ablation. Advanced Functional Materials (2026): e75094.
原文链接:https://doi.org/10.1002/adfm.75094
论文作者:邱硕(一作),吴云娣(一作),刘若灿(一作),曲焕然,邵世洋,陈建强,吴锡龙(通讯)
作者单位:海南大学生物医学工程学院,海南大学药学院,海南大学材料科学与工程学院,海南医科大学第一附属医院
资助项目:国家自然科学基金、海南省南海育才南海创新人才计划教育领域项目、海南省重点研发项目、海南省自然科学基金创新研究团队项目等。
 公安部备案号:46010802000190 Copyright © 2024 hainan university
公安部备案号:46010802000190 Copyright © 2024 hainan university




